近日,《美国国家科学院院刊》(PNAS)在线发表了由白津教授团队完成的研究成果。青年教师杨文栋、研究生卢梦茹和沈琦为该论文的共同第一作者,白津教授、葛文杰教授和浙江省肿瘤医院的邵智颖副主任为共同通讯作者。
结直肠癌是全球高发恶性肿瘤,临床仍面临耐药与治疗瓶颈。近年来,铜死亡(Cuproptosis)—— 一种依赖铜离子过载、靶向线粒体三羧酸循环关键蛋白的新型程序性细胞死亡方式,成为肿瘤治疗研究热点。但肿瘤细胞如何调控铜死亡、能否安全可控地用于抗癌,一直是未解难题。
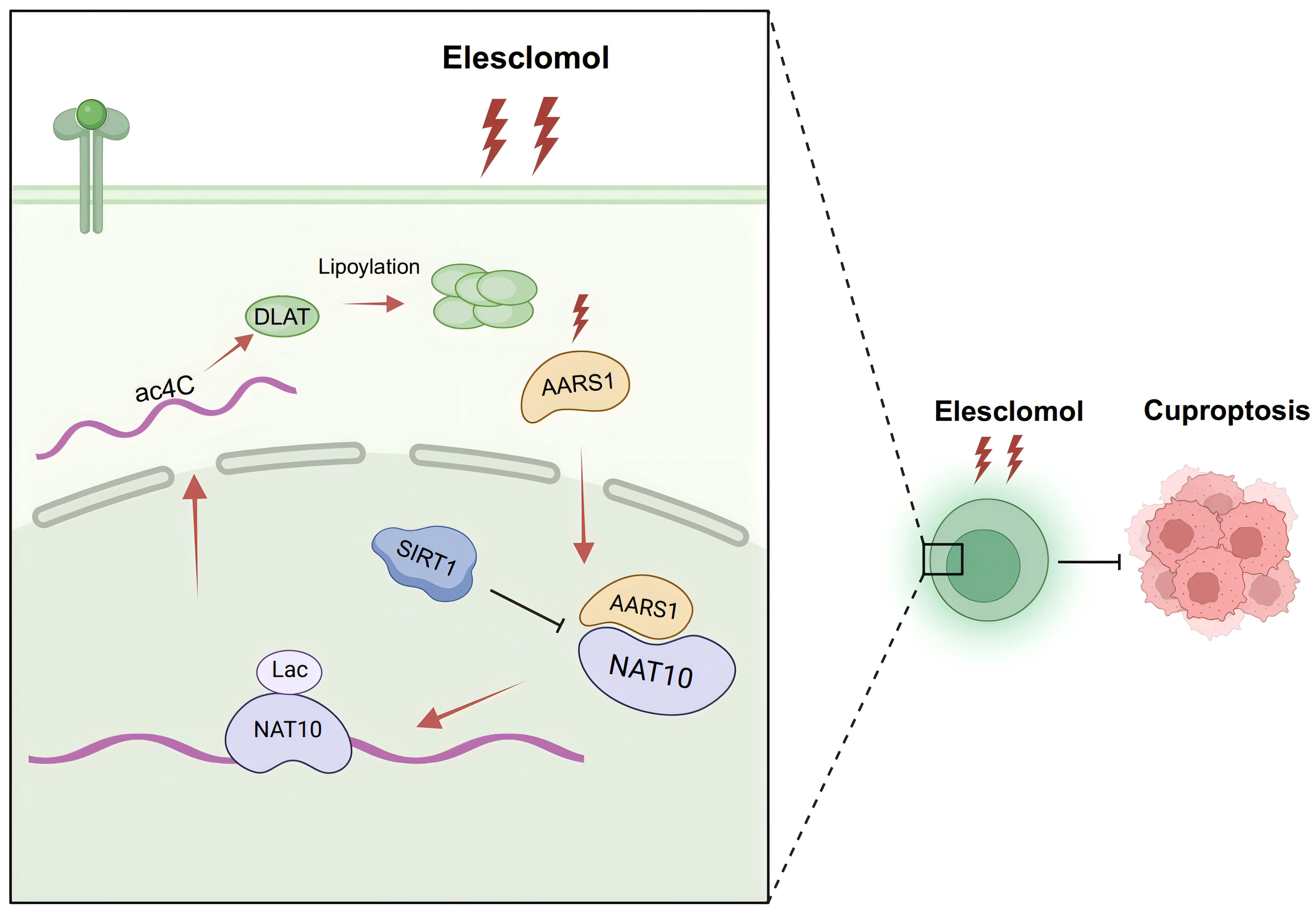
研究团队首先在临床样本中证实:结直肠癌组织铜含量与结直肠癌恶性表型呈现明显的正相关。在此基础上,团队展开机制攻关,取得一系列原创发现。研究发现之一:NAT10是结直肠癌铜死亡的核心开关。作为唯一已知的RNA乙酰化(ac4C)修饰酶,NAT10在结直肠癌中显著高表达,并通过催化DLAT mRNA的ac4C修饰增强其稳定性,进而上调DLAT蛋白水平,促进铜死亡发生。研究发现之二: NAT10的K426位点乳酸化是“激活钥匙”。铜死亡诱导剂Elesclomol处理后,NAT10蛋白与mRNA水平不变,但第426位赖氨酸(K426)的乳酸化修饰大幅上升,直接增强NAT10的催化活性,形成“上游激活—下游放大”的高效通路。研究发现之三: 正反馈环路持续放大抗癌效应。Elesclomol引发铜死亡时,可溶性DLAT减少会进一步促进NAT10-K426乳酸化,形成NAT10/ac4C/DLAT正反馈环,持续“加料”推动铜死亡,实现高效、不可逆的肿瘤细胞杀伤。
该团队首次揭示乳酸化修饰的NAT10通过NAT10/ac4C/DLAT正反馈环路,驱动铜死亡杀伤结直肠癌细胞的全新机制,并证实铜离子载体Elesclomol联合SIRT1抑制剂Selisistat可协同强效诱导铜死亡,为晚期结直肠癌提供了极具转化前景的联合治疗新策略。

(一审:姜嘉,二审:许璐璐,三审:于宁波)
