近日,徐州医科大学血液病研究所在血小板产生领域取得重要进展。相关研究成果以“Notch1 regulates hepatic thrombopoietin production”为题,发表在血液学领域顶级期刊Blood(IF=21,中科院1区Top期刊)。
血小板生成素(TPO)参与调控巨核细胞分化和血小板产生。TPO主要在肝脏合成,其水平的异常参与多种疾病的发生和发展。在正常生理状况下,体内衰老去唾液酸化血小板通过与肝细胞表面的Ashwell-Morell receptor(AMR)受体结合调控肝细胞TPO的合成和分泌。但目前关于调控肝细胞TPO产生的机制研究较少。
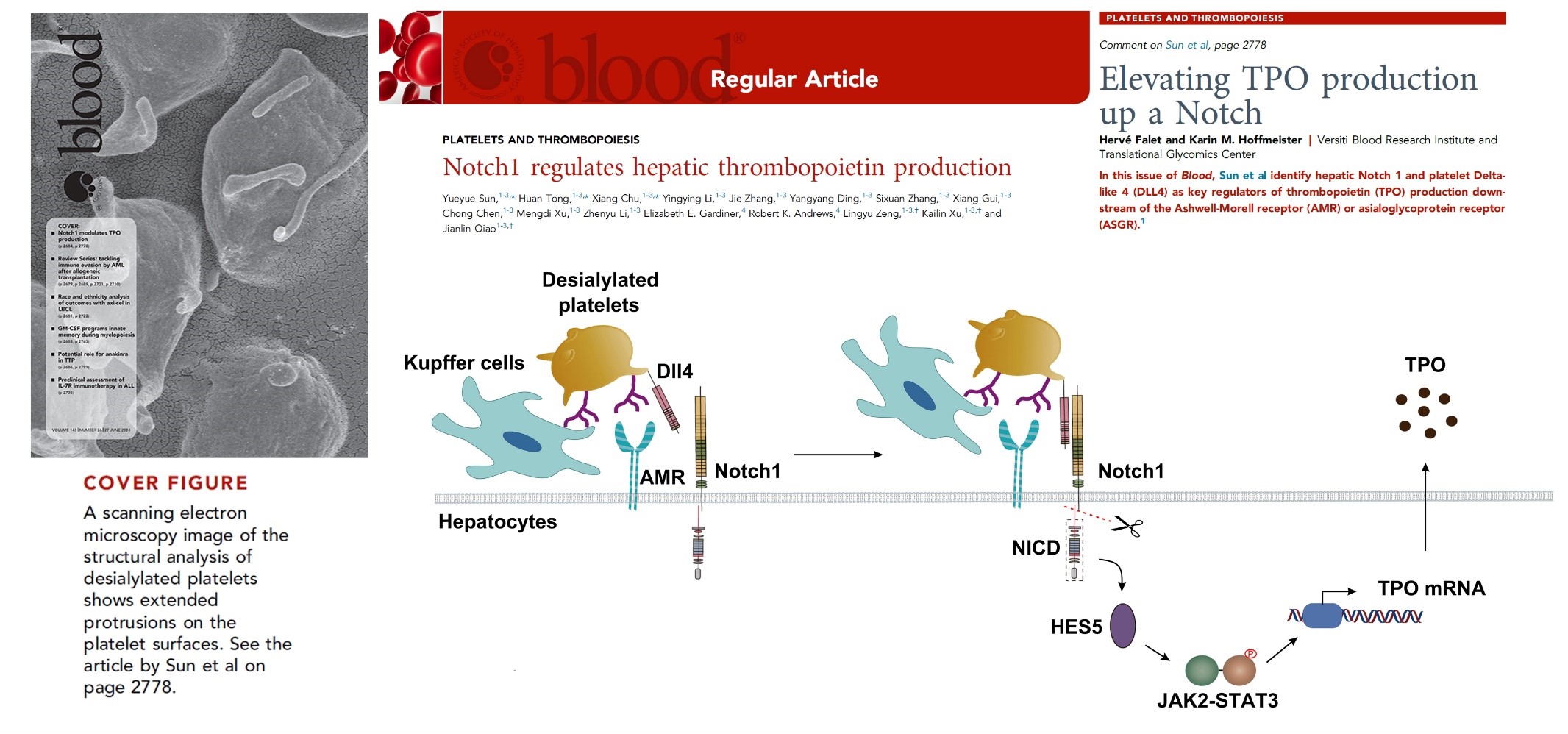
该研究利用肝细胞特异性Notch1敲基因小鼠发现敲除肝细胞Notch1显著降低小鼠血小板的数目及血浆和肝脏TPO的表达水平。同时,肝细胞Notch1敲除小鼠骨髓中巨核细胞的成熟和分化状态显著受到抑制,而额外补充TPO则可促进Notch1敲除小鼠骨髓中巨核细胞的分化和增加外周循环中血小板的数目。RNA-Seq分析小鼠肝脏标本发现多种表达差异基因。KEGG通过富集分析发现这些表达差异的基因富集在JAK-STAT信号通路。与此一致,Notch1敲除的原代肝细胞内JAK2/STAT3的磷酸化水平显著降低。此外,Notch1敲除后显著抑制了去唾液酸化血小板介导的肝细胞内TPO的合成及下游靶基因Hes5的表达。机制研究发现,去唾液酸化血小板引起肝细胞内Hes5与JAK2/STAT3结合,进而介导STAT3的磷酸化,调控肝细胞内TPO的转录和翻译。进一步研究发现,肝细胞AMR受体与去唾液酸化血小板结合促进肝细胞内Notch1信号通路的活化。同时,去唾液酸化血小板表面表达的Dll4通过与肝细胞表面的Notch1受体结合,引起Notch1信号通路的活化和靶基因Hes5的表达,进而调控STAT3磷酸化和TPO合成。本项研究揭示了Notch1在调控正常生理状态下肝脏合成TPO中的关键作用,提示其可能是调控体内TPO水平的关键靶点,为TPO水平异常相关疾病的治疗提供潜在策略。
上述工作得到了美国Versiti 血液研究所和转化糖组学中Hervé Falet和Karin M. Hoffmeister教授的点评(Blood Commentary),高度评价和赞扬了该研究工作,指出该研究工作填补了AMR是通过何种机制参与调控肝细胞TPO的产生这一空白,加深了对生理状况下肝细胞TPO产生调控机制的认识和理解,为进一步调节体内TPO的水平提供了一种新的选择。
论文通讯单位为徐州医科大学血液病研究所/徐州医科大学附属医院血液科。徐州医科大学附属医院血液科孙月月医师、徐州医科大学硕士研究生童欢和褚翔为论文共同第一作者,徐州医科大学血液病研究所乔建林教授、徐开林教授和曾令宇教授为论文共同通讯作者。该研究得到了国家自然科学基金优秀青年基金、国际合作项目和面上项目资助。
原文链接:https://doi.org/10.1182/blood.2023023559
